Pacjenci znają hormon antymüllerowski (AMH) głównie z tego, że jest uważany za najlepszy marker rezerwy jajnikowej, czyli że pozwala ocenić płodność kobiety np. przy rozpoczęciu procedury in vitro. Jednak AMH coraz częściej interesuje też onkologów pod kątem jego potencjału w diagnozowaniu i leczeniu różnych nowotworów.
Międzynarodowy zespół badaczy opublikował właśnie w czasopiśmie „Frontiers in Endocrynology” artykuł przeglądowy na temat biologii hormonu antymüllerowskiego oraz jego roli w endokrynologii i onkologii. Pierwszym autorem publikacji jest dr n. med. Marek Gowkielewicz, ginekolog z Wydziału Lekarskiego Collegium Medicum Uniwersytetu Warmińsko-Mazurskiego w Olsztynie. Wśród współautorów jest również prof. Carsten Carlberg, kierownik Pracowni Nutrigenomiki w Instytucie Rozrodu Zwierząt i Badań Żywności PAN w Olsztynie.
Przegląd porządkuje aktualną wiedzę na temat AMH, badając jego rolę na różnych etapach życia: od rozwoju płodu, dzieciństwa i dojrzewania, po jego zaangażowanie w podwzgórze, przysadkę mózgową, funkcję jajników i menopauzę. Naukowcy badają również znaczenie AMH w technologiach reprodukcyjnych, takich jak kriokonserwacja tkanki jajnika oraz jego następstwa dla cyklu komórkowego i biologii raka.
Jak bowiem tłumaczy prof. Carsten Carlberg, AMH ma wieloraki i złożony wpływ na rozwój i funkcję różnych ludzkich tkanek.
Obecnie AMH jest najczęściej stosowany do pomiaru rezerwy jajnikowej, która pozwala zbadać płodność kobietypoprzez ocenę zdolności jajników do dostarczania żywotnych komórek jajowych. Jest to szczególnie istotne w leczeniu niepłodności, np. przy procedurze in vitro, gdzie poziom AMH jest sprawdzany w celu optymalizacji szans na sukces.
Jednak ze względu na zdolność AMH do hamowania cyklu komórkowego i indukowania apoptozy (procesu inicjowania zaprogramowanej śmierci komórki) coraz częściej interesuje również onkologów.
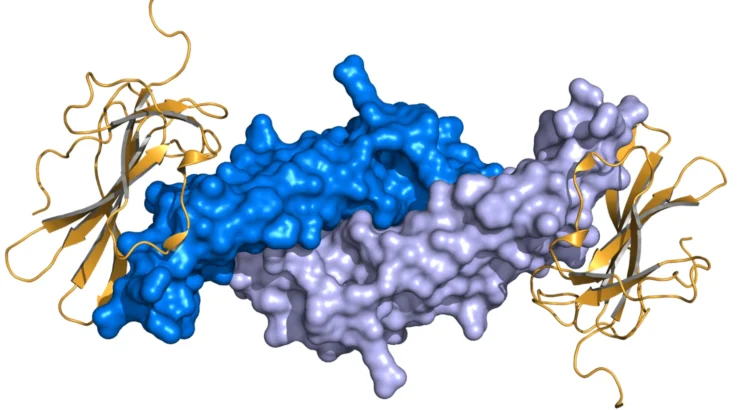
– Jeden z obiecujących obszarów badań koncentruje się na przeciwciałach ukierunkowanych na receptor AMH – AMHR2, który odgrywa kluczową rolę w sygnalizacji i modulowaniu ekspresji setek genów. Badania na modelu zwierzęcym wykazały, że przeciwciała skoniugowane (sprzężone) z radioaktywnym izotopem, które celują w AMHR2 wykazały potencjał w niszczeniu komórek nowotworowych – wyjaśnia prof. Carsten Carlberg.
Ponadto, AMH wykazuje ochronny i pozytywny wpływ na rezerwę jajnikową przed zastosowaniem chemioterapii, która jest toksyczna dla tkanki jajnika. – A ponieważ AMH stabilizuje pulę pierwotnych pęcherzyków jajnikowych, może też zwiększyć odporność tkanki jajnika na szkodliwe warunki procedur kriokonserwacji, czyli procesu zamrażania – mówi badacz.
Dodatkowo, AMH jest obecny w neuronach ruchowych, gdzie działa jako ochronny czynnik wzrostu, potencjalnie wpływając na procesy uczenia się i pamięci. – Doprowadziło to do spekulacji, że AMH może wspierać leczenie chorób neurodegeneracyjnych, takich jak choroba Alzheimera – dodaje prof. Carsten Carlberg.
Znane nauce są również powiązania między AMH a rakiem jajnika i endometrium, choć tu pozostaje jeszcze wiele do odkrycia.
– Pomimo licznych badań i zdobytej wiedzy, potrzebne są jednak dalsze badania, ponieważ pełny potencjał AMH jest nadal niejasny. Dzisiejsza wiedza na temat AMH jest wykorzystywana przez specjalistów od płodności, a także daje nadzieje na przyszłe zastosowania w onkologii – podsumowuje prof. Carsten Carlberg.
—
Prof. Carsten Carlberg to światowej sławy biochemik specjalizujący się w badaniach nad witaminą D. Jest liderem grupy naukowej zajmującej się nutrigenomiką w Instytucie Rozrodu Zwierząt i Badań Żywności PAN w Olsztynie, powołanej w ramach projektu ERA Chair WELCOME2 (Horyzont2020).
Więcej o działaniach zespołu na stronie: https://welcome2.pan.olsztyn.pl/.